Nuevo ‘medicamento huérfano’ contra la ‘piel de mariposa’. Un producto de bioingeniería tisular basado en el empleo de células de paciente corregidas mediante edición genómica ha sido designado como medicamento huérfano por la Agencia Europea del Medicamento (EMA) para el tratamiento de la Epidermólisis Bullosa Distrófica Recesiva.
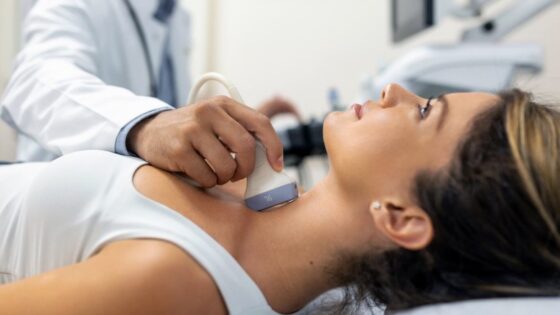
Se caracteriza por la aparición de fragilidad en la piel y mucosas, úlceras y carcinomas cutáneos agresivos
Dicha enfermedad, conocida también como piel de mariposa, se caracteriza por la aparición de fragilidad en la piel y mucosas, úlceras y carcinomas cutáneos agresivos.
Los trabajos para conseguir esta designación, patrocinada por el Centro de Investigación Biomédica en Red de Enfermedades Raras (CIBERER), han sido coordinados por Fernando Larcher desde el grupo que lidera Marcela del Río; el Centro de Investigaciones Energéticas, Medioambientales y Tecnológicas (CIEMAT) y la Universidad Carlos III de Madrid (UC3M); en colaboración con el Instituto de Investigación Sanitaria de la Fundación Jiménez Díaz (IIS-FJD) y el Centro Comunitario de Sangre y Tejidos de Asturias (CCST).

Un desafío para profesionales de la salud
La Epidermólisis Bullosa Distrófica Recesiva es una enfermedad rara caracterizada por la formación continua de erosiones y ampollas en piel y mucosas internas, así como fibrosis y diversas complicaciones como la pseudosindactilia (fusión de los dedos) y una alta predisposición al desarrollo de carcinoma epidermoide metastásico.
Esta enfermedad supone un desafío para los profesionales de la salud y un gran esfuerzo para los pacientes y sus familias
El manejo de esta enfermedad supone un desafío para los profesionales de la salud y un gran esfuerzo para los pacientes y sus familias.
Esta enfermedad, de base genética, está causada por mutaciones en el gen COL7A1, que codifica para el colágeno 7, una proteína esencial para la adhesión de la epidermis a la dermis.

Seguridad biológica y eficacia terapéutica
En España, existe una alta prevalencia de una mutación que se localiza en el exón 80 del gen (presente en aproximadamente el 50 por ciento de los pacientes españoles), lo que justifica el desarrollo de una terapia de precisión dirigida a esta región del gen.
Hasta el desarrollo de este producto las herramientas moleculares CRISPR/Cas9 carecían de los niveles de eficacia necesarios para una aplicación clínica realista en células madre adultas tales como las hematopoyéticas o cutáneas. Así pues, estas estrategias no podían competir con las terapias génicas convencionales de adición empleando vectores virales.
Este producto de terapia avanzada, que hace uso de la herramienta CRISPR/Cas9 de forma altamente eficaz, fue validado con éxito en un modelo preclínico de la enfermedad y publicado en 2019 en la revista Molecular Therapy.

Ciberer y diez medicamentos huérfanos
El Ciberer ha promovido ya, con este, diez medicamentos huérfanos que han sido designados por la Agencia Europea del Medicamento (EMA), cuatro de los cuales también han sido designados como tales por la agencia americana (FDA).
El Ciberer ha promovido diez medicamentos huérfanos que han sido designados por la Agencia Europea del Medicamento (EMA)
La designación como medicamento huérfano por parte de la EMA tiene ventajas como la de recibir una autorización de comercialización durante una década en la que no pueden comercializarse productos similares, poder disponer de protocolos de asistencia y consejo científico gratuitos o con un coste reducido, y la exención de pagos para la designación.
Además, las entidades que desarrollan medicamentos huérfanos tienen acceso a subvenciones específicas de la Unión Europea y de los programas de los estados miembros.
Recuerda que conideintelligente.com solo te ofrece información de fuentes oficiales y de profesionales sanitarios.